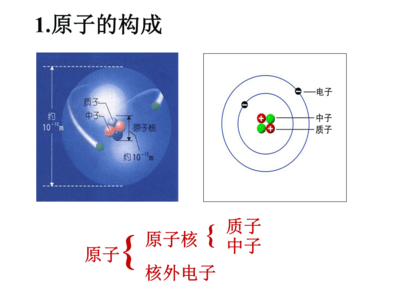
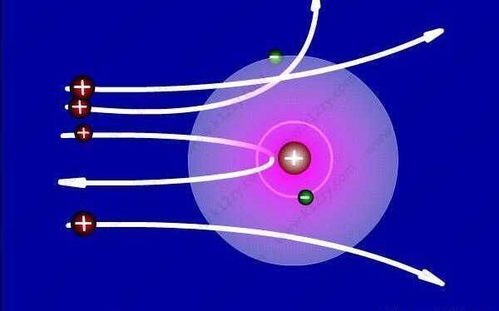
原子核外電子的排布并非雜亂無章,而是遵循著一系列基本的物理規律。理解這些規律是掌握原子結構與元素性質關系的關鍵。
一、電子排布遵循的基本原則
- 能量最低原理:電子總是優先占據能量最低的軌道,以使整個原子體系處于能量最低、最穩定的狀態。電子填充軌道的順序遵循構造原理,即從1s軌道開始,按能級組由低到高依次填充。
- 泡利不相容原理:在同一個原子中,不可能存在運動狀態完全相同的兩個電子。換言之,每一個原子軌道最多只能容納兩個自旋方向相反的電子。
- 洪特規則:當電子在能量相同的軌道(即簡并軌道,如三個p軌道、五個d軌道)上排布時,總是優先以自旋方向相同的方式,單獨占據不同的軌道。這種排布方式使原子的能量最低、最穩定。洪特規則的特例是,對于同一電子亞層,當電子排布處于全充滿、半充滿或全空狀態時,原子體系比較穩定。
二、核外電子排布的表示方法
- 原子結構示意圖:用圓圈表示原子核及核電荷數,用弧線表示電子層,弧線上的數字表示該層上的電子數。這是一種直觀但不夠精確的表示方法。
- 電子排布式:這是最常用且精確的表示方法。它按能級順序寫出各亞層符號,并在其右上角用數字標出該亞層上的電子數。例如,鈉原子(Na,原子序數11)的電子排布式為:1s22s22p?3s1。對于部分原子,為簡化書寫,常用其前一周期的稀有氣體元素符號加方括號表示內層電子構型,如鈉也可表示為[Ne]3s1。
- 軌道表示式(又稱電子排布圖):用小方格(或圓圈)代表原子軌道,用箭頭(↑和↓)表示電子的自旋狀態。它能更直觀地體現洪特規則和泡利原理。
三、電子排布與元素周期律
核外電子排布的周期性變化是元素性質(如原子半徑、電離能、電負性等)呈現周期性變化的根本原因。主族元素的價電子排布(即最外層電子排布)決定了其主要的化學性質。例如,堿金屬元素的最外層都是ns1結構,易于失去一個電子形成+1價陽離子,表現出強烈的金屬性。
掌握原子核外電子排布的規律,不僅能幫助我們書寫任意原子的電子構型,更是理解元素在周期表中的位置、預測元素及其化合物物理化學性質的理論基石。